Wyszukaj w wideo
Diagnostyka genetyczna kardiomiopatii okiem diagnosty laboratoryjnego
I Międzynarodowy Kongres Kardiomiopatii - I dzień
Podczas I Międzynarodowego Kongresu Kardiomiopatii znakomici eksperci omówili najważniejsze zagadnienia dotyczące leczenia i diagnostyki tych schorzeń. Jakie trudności niesie ze sobą kompleksowa opieka nad pacjentem zmagającym się z kardiomiopatią?
Odcinek 9
Dr n. med. Dorota Czapczak przedstawiła spojrzenie diagnosty laboratoryjnego na diagnostykę genetyczną kardiomiopatii.Prelegentka zaznaczyła, iż wprowadzenie NSG umożliwiło identyfikację kilkudziesięciu genów związanych z patogenezą kardiomiopatii. W dalszej części podkreśliła znaczący wpływ badań genetycznych na sposób postępowania profilaktyczno-terapeutycznego, również u chorych będących w okresie bezobjawowym.
Dzień dobry państwu.Bardzo serdecznie dziękuję organizatorom MiędzynarodowegoKongresu Kardiomiopatii za zaproszenie i możliwośćwygłoszenia wykładu na temat: diagnostykagenetyczna kardiomiopatii okiem diagnosty laboratoryjnego.
Ocenia się, że kardiomiopatiewystępują z częstością jeden na średniojeden na sześć tysięcy siedemseturodzeń.I wśród kardiomiopatii wrodzonychwyróżniamy kardiomiopatie izolowane i kardiomiopatie syndromiczne.Kardiomiopatie izolowane to przede wszystkimkardiomiopatia przerostowa, kardiomiopatia rozszczeniowa i najrzadziejwystępująca kardiomiopatia restrykcyjna.Kardiomiopatie syndromiczne występują jako objawchorób monogenowych dziedziczonych zgodnie z prawamiMendla, takich jak na przykładataksja Friedreicha, glikogenozy, choroba Danona, chorobaFabry'ego, dystrofia miotoniczna, dystrofia mięśniowaDuchenne'a, pląsawica Huntingtona czy zespół Alstroma.Kardiomiopatie również mogą być objawemchorób rzadkich, takich jak rasopatie, naprzykład zespół Noonan czy zespółCostello, czy też zespół sercowo-twarzowo-skórny.Mogą być również objawem choróbmitochondrialnych.
Kardiomiopatie najczęściej dziedziczą się wsposób autosomalny, dominujący, ale obserwujemy równieżinne wzory dziedziczenia, to znaczydziedziczenie autosomalnie recesywne, jak również dziedziczeniesprzężone z chromosomem X orazdziedziczenie mitochondrialne.
Kardiomiopatie wrodzone mają podłoże heterogenne.Zdarza się także różne warianty,w różnych genach powodują ten samfenotyp u pacjenta i odwrotniejeden wariant w tym samym genie,tak naprawdę u kilku członkówtej samej rodzinie, rodziny może powodowaćróżne fenotypy, różne typy kardiomiopatiio różnym nasileniu.Wynika to prawdopodobnie z tego,że taki wariant ma niepełną, niepełnąpenetrację i zmienną ekspresję, adodatkowo mogą tutaj występować tak zwanemodyfikatory, które mogą nasilać lubosłabiać wariant sprawczy.Mogą to być na przykładmikro RNA albo dodatkowe warianty winnych, w innych genach.
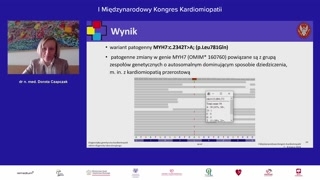
Jeśli chodzi o kardiomiopatię przerostową,to najczęściej w pięćdziesięciu tak naprawdęprocentach obserwujemy warianty patogenne wgenie MYH7 i w genie MYBT3.Obecnie znamy około tak naprawdęsześćdziesięciu genów, w których mutacje mogąodpowiadać za wystąpienie kardiomiopatii przerostowej.W przypadku kardiomiopatii rozszczeniowej najczęś-najczęściejsą to warianty w genie titiny,w genie miozyny, miozyny iw genie laminy.Ale tutaj również obserwujemy wariantyw innych, w innych genach.W związku z tym, żekardiomiopatie mają heterogenne podłoże, metodą zwyboru tak naprawdę jest sekwencjonowanienastępnej generacji, które umożliwia badanie wielu
genów w jednym badaniu.Nadal jednak złotym standardem jestsekwencjonowanie metodą Sangera i tak naprawdękażdy wariant wykryty metodą NGSpowinien być potwierdzony sekwencjonowaniem Sangera.Jeśli nie wykryjemy wariantu sprawczegometodą NGS, to znaczy wariantów punktowych,ewentualnie małych delecji, można rozważyćwykonanie badania metodą mikromacierzy lub MLPAw celu poszukiwania wariantów zmianyliczby kopii.
Nasza pracownia, Pracownia Chorób Rzadkichod lipca ubiegłego roku jest wstrukturze nowej jednostki, to znaczyLaboratorium Genetyki UCML-u, którego kierownikiem jestprofesor Tomasz Stokłosa.Wcześniej pracownia występowała jako pracowniagenetyki, była w strukturze Zakładu DiagnostykiLaboratoryjnej i Immunologii Klinicznej WiekuRozwojowego, którego kierownikiem była Pani profesorUrszula Demkow.Pracownia, tak jak Pan profesorKrzysztof Szczołba wspomniał, współpracuje z PoradniąGenetyczną i z Klinikami KardiologiiDziecięcej, Kliniką Kardiologii CSK, Kliniką KardiologiiSKDJtu i Kliniką Chorób Wewnętrznychna Ciśnienia Tętniczego i Angiologii CSK.
W ramach tej współpracy wykonujemywłaśnie badania, między innymi badania genetyczneu pacjentów z chorobami sercowo-naczyniowymi,w tym u pacjentów z kardiomiopatiami. Głównymcelem badania genetycznego jest przedewszystkim identyfikacja mutacji patogennej wariantu sprawczegoodpowiedzialnego za wystąpienie choroby orazsegregacja wariantów w rodzinie i wykluczeniechoroby u krewnych bez mutacjioraz lub potwierdzenie nosicielstwa patogennego wariantuu bezobjawowych krewnych, co jestbardzo istotne i objęcie ich opiekąlekarską.Tak jak wspomniałam, ponieważ kardiomiopatie
mają podłoże heterogenne, metodą z wyborujest sekwencjonowanie następnej generacji.My wykorzystujemy badanie panel truceitecardio do-- truceite cardio tak naprawdę,dzięki któremu możemy przeanalizować sekwencjekodujące stu siedemdziesięciu czterech genów, wtym kilkudziesięciu genów powiązanych zkardiomiopatiami.Materiałem do badania jest DNAwyizolowane z leukocytów krwi obwodowej.Kolejnym etapem jest przygotowanie bibliotek,następnie sekwencjonowanie, analiza danych i generowaniewyników.
Analiza danych to proces kilkuetapowy.Pierwszy etap to jest generowanieplików fastku, które następnie są konwertowanedo plików BAM, a tez kolei konwertowane do plików VCF.Następnie jest adnotacja i filtrowaniewariantów i wybór wariantu sprawczego, któryodbywa się na podstawie dostępnychbaz danych, programów predykcyjnych i dostępnejliteratury.Tutaj należy zwrócić uwagę, żewyniki analiz predykcyjnych nie zastąpią badańfunkcjonalnych, które niestety nie sądostępne w laboratoriach diagnostycznych.
Ważną sprawą jest prawidłowy zapiswyniku, który powinien być zgodny znomenklaturą HGVS, ponieważ błędny zapiswariantu spowoduje badanie innej mutacji niżwariant markerowy w rodzinie, zbadanie--zlecenie badania innej sekwencji, a coza tym idzie nieprawidłową poradęgenetyczną.Ocena wykrytego wariantu powinna byćzgodna z klasyfikacją ACMG.Obecnie mamy pięciostopniową klasyfikację.Wypisujemy warianty tylko patogenne iprawdopodobnie patogenne.Warianty o niepewnym znaczeniu klinicznym
wypisujemy tylko w powiązaniu, jeśli jestkorelacja z fenotypem pacjenta.Do chwili obecnej wykonaliśmy badaniepanelem truceite cardio u czterystu trzechpacjentów, z czego trzydzieści procentstanowili pacjenci z kardiomiopatiami.Głównie byli to pacjenci zkardiomiopatią przerostową i rozstrzeniową.Wydaliśmy dwadzieścia sześć procent wynikównieprawidłowych, czterdzieści trzy niejednoznacznych i trzydzieściprocent wyników prawidłowych.
I taki przykład, do klinikikardiologii dziecięcej została skierowana jedenastoletnia dziewczynkaze szpitala rejonowego z powodunieprawidłowego wyniku EKG obniżonej tolerancji wysiłku.U pacjentki podejrzewano zespół WolfaParkinsona White'a.Wykonano echo serca, które wykazałokardiomiopatię przerostową.Poza tym były podwyższone badania--w badaniach laboratoryjnych stężenie kinazy kreatynoweji troponiny.Pacjentkę skierowano na panel truceite--panel genetyczny truceite cardio.W wyniku tego badania stwierdziliśmywariant, który w genie LAMP2, którypowoduje wariant nonsensowny, który powodujepowstanie-- przedwczesną terminację translacji, powstanie kodomustop, powstanie białka kadłubowego.Patogenne warianty w genie LAMPodpowiedzialne są za wystąpienie choroby Danonasprzężonej do-- sprzężonej, dziedziczonej wsposób dominujący sprzężony z chromosomem X.Tak naprawdę jest to jedynachoroba spichrzeniowa, właśnie dziedziczona w sposóbdominujący, sprzężony z chromosomem X.Objawem tej choroby jest międzyinnymi kardiomiopatia przerostowa i zespół WolffaParkinsona White'a.
Dziewczyn-- wykonano segregację wariantu wrodzinie.Rodzice i siostra pacjentki sązdrowi.Nie stwierdzono wariantu u krewnychpacjentki.Obecnie dziewczynka jest po wszczepieniukardiowertera.
I kolejny przykład.Piętnastomiesięczne niemowlę trafia do klinikikardiologii z powodu stwierdzonej kardiomiopatii przerostowejw badaniu prenatalnym.Dziecko skierowano na badanie genetycznepanelem truceite cardio.U dziecka stwierdzono wariant wgenie MYH7.Wariant został wypisany jako wariantniejednoznaczny z racji na to, żenie było dostępnych danych natemat tego wariantu ani w literaturze,ani w bazach danych.W związku z tym wtakiej sytuacji najlepsza jest segregacja wariantuw rodzinie.Wykonaliśmy badanie u rodzeństwa iwariant stwierdzono u chorej siostry, dziesięcioletniejsiostry probanta i wykluczono wariantu zdrowej siostry probanta.Poza tym wariant został jeszcze--odbyła się segregacja wariantu u rodzicówi krewnych drugiego i trzeciegostopnia.Badania zostały wykonane w Instytuciew Aninie, gdzie stwierdzono wariant jeszczeu ośmiu krewnych.Wszyscy byli-- mieli kardiomiopatię przerostową,dwie osoby miały łagodniejszy przebieg kardiomiopatii.
I takie podsumowanie na koniec,wprowadzenie sekwencjonowania następnej generacji umożliwia identyfikacjękilkudziesięciu genów związanych z patogeneząkardiomiopatii.Mutacje w tych genach mogąbyć przyczyną izolowanych lub syndromicznych kardiomiopatii.Wyniki badań genetycznych w diagnostycekardiomiopatii mają przełożenie na sposób postępowaniadiagnostycznego, profilaktyczno-terapeutycznego pacjentów, również wokresie bezobjawowym.Dlatego tak ważna jest diagnostykanawet bezobjawowych krewnych, u których-- krewnychprobanta, u którego stwierdzono wariantpatogenny.Tym bardziej, że kardiomiopatia bardzoczęsto objawia się w wieku młodzieńczymlub u młodych dorosłych.Bardzo dziękuję mojemu zespołowi, któryjest zaangażowany w badania genetyczne idziękuję Państwu za uwagę izapraszam do współpracy.
Rozdziały wideo

Wprowadzenie i klasyfikacja kardiomiopatii

Genetyczne podłoże i najczęstsze geny kardiomiopatii

Metody diagnostyki genetycznej i organizacja pracowni

Przygotowanie próbek, analiza danych i interpretacja wariantów

Wyniki badań oraz przypadek choroby Danona