Wyszukaj w publikacjach
Miopatie zapalne – gdy ból i osłabienie mięśni to coś więcej niż przemęczenie

Miopatie zapalne to heterogenna grupa chorób autoimmunologicznych, których wspólną cechą jest przewlekły proces zapalny prowadzący do uszkodzenia mięśni szkieletowych. Objawy często rozpoczynają się niespecyficznie – narastającym osłabieniem, bólem lub zmęczeniem mięśni – co może utrudniać rozpoznanie.
Klasyfikacja i epidemiologia miopatii zapalnych
Miopatie zapalne należą do rzadkich chorób układowych o częstości ok. 5–10 przypadków na 100 000 osób. Chorują głównie kobiety w średnim wieku, choć odmiany skórno-mięśniowe występują również u dzieci.
Najczęstsze typy miopatii zapalnych to:
- zapalenie wielomięśniowe (polymyositis, PM) – typowo bez zmian skórnych, z symetrycznym osłabieniem mięśni proksymalnych;
- zapalenie mięśniowo-skórne (dermatomyositis, DM) – z charakterystycznymi zmianami skórnymi (rumień heliotropowy, objaw Gottrona), niekiedy o charakterze paraneoplastycznym;
- zapalenie mięśni z ciałkami wtrętowymi (IBM) – przewlekłe, oporne na leczenie, częściej u mężczyzn >60. r.ż.;
- autoimmunologiczne nekrotyzujące zapalenie mięśni (IMNM) – ciężka postać, często z obecnością autoprzeciwciał anty-SRP lub anty-HMGCR, związana także z terapią statynami;
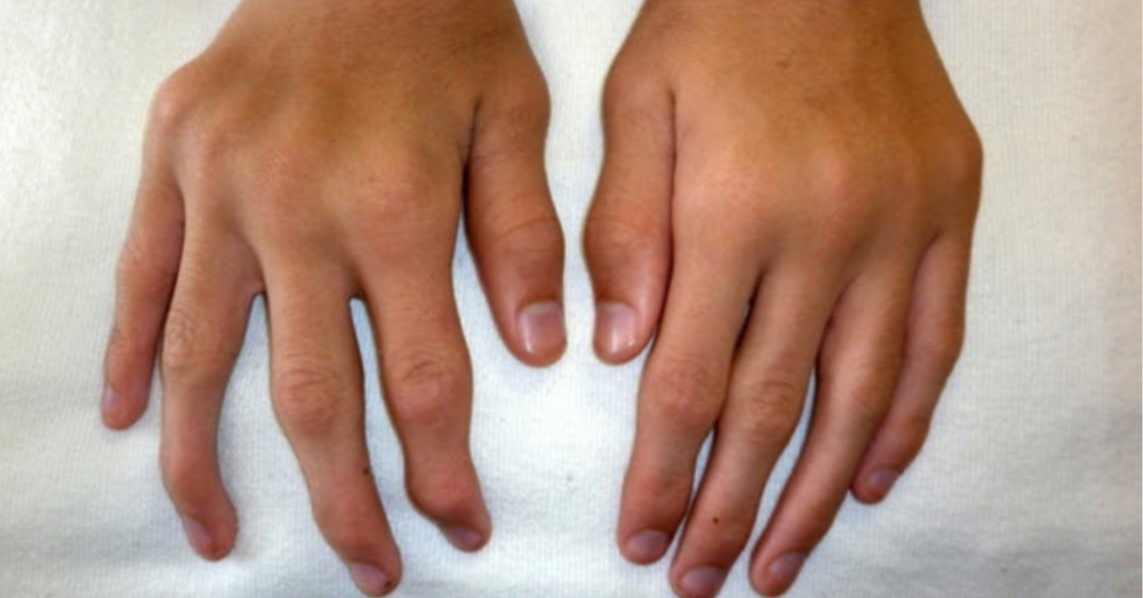
- zespół antysyntetazowy (ASSD) – postać zapalenia mięśni związana z obecnością autoprzeciwciał przeciwko syntetazom tRNA (najczęściej anty-Jo-1); charakteryzuje się triadą objawów: zapaleniem mięśni, śródmiąższową chorobą płuc (ILD) oraz objawami reumatologicznymi lub naczyniowymi (artropatia, objaw Raynauda, „ręce mechanika”).
Objawy miopatii zapalnych – jak rozpoznać chorobę mięśni
Najczęstszym objawem jest symetryczne osłabienie mięśni proksymalnych – obręczy barkowej i biodrowej – powodujące trudności w wchodzeniu po schodach, wstawaniu z krzesła, unoszeniu rąk. Często współwystępują:
- bóle mięśniowe, sztywność i męczliwość,
- zaburzenia połykania (dysfagia) – wynik zajęcia mięśni gardła,
- objawy ogólne – gorączka, spadek masy ciała, uczucie przewlekłego zmęczenia,
- w DM – charakterystyczne zmiany skórne.
W zaawansowanych przypadkach pojawia się zajęcie mięśni oddechowych, prowadzące do duszności, oraz miopatia sercowa z zaburzeniami rytmu.
Jednostka chorobowaDodatkowe objawy i zajęcie układów pozamięśniowychdermatomyositis
- zmiany skórne (rumień heliotropowy, grudki Gottrona, objaw szala)
- zajęcie płuc – śródmiąższowa choroba płuc (ILD)
- dysfagia, refluks, rzadziej zajęcie serca
- u dorosłych – możliwość współistnienia nowotworu
polymyositis
- ILD
- zaburzenia rytmu i kardiomiopatia
- dysfagia wynikająca z zajęcia mięśni gardła
- objawy ogólne: gorączka, spadek masy ciała
zespół antysyntetazowy
- ILD (najczęstsze powikłanie, czasem dominujące)
- artropatia przypominająca RZS
- „ręce mechanika” (szorstka, pękająca skóra dłoni)
- objaw Raynauda, gorączka, wysypka rumieniowa twarzy
autoimmunologiczne nekrotyzujące zapalenie mięśni
- znacznie nasilona miopatia, czasem z rabdomiolizą
- możliwe zajęcie serca (arytmie, kardiomiopatia)
- często brak zmian skórnych i objawów układowych
zapalenie mięśni z ciałkami wtrętowymi
- przewlekłe, postępujące osłabienie mięśni
- często dysfagia
- rzadko zajęcie płuc lub serca, ale możliwe współistnienie neuropatii obwodowej
młodzieńcze zapalenie skórno-mięśniowe
- zwapnienia podskórne
- zapalenie naczyń skóry i przewodu pokarmowego
- dysfagia, refluks
- zazwyczaj brak związku z nowotworem
Diagnostyka miopatii zapalnych – badania laboratoryjne i obrazowe
Rozpoznanie miopatii zapalnej opiera się na korelacji objawów klinicznych, wyników laboratoryjnych i badań obrazowych lub histopatologicznych. Podejrzewając miopatię zapalną, należy skierować chorego na oddział reumatologii celem pogłębienia diagnostyki.
- Badania laboratoryjne:
- zwiększenie aktywności enzymów mięśniowych: CK (często >10× norma), AST, ALT, LDH, aldolaza,
- obecność autoprzeciwciał specyficznych dla miopatii (MSA) lub towarzyszących (MAA), np.:
- anty-Jo-1, anty-PL-7, anty-PL-12 – zespół antysyntetazowy,
- anty-Mi-2 – typowe dla DM,
- anty-SRP i anty-HMGCR – IMNM,
- anty-TIF1-γ, anty-NXP2 – DM związane z nowotworem.
- Badania obrazowe:
- MRI mięśni – ocena obszarów zapalenia i włóknienia (sygnał T2/STIR), przydatne także do wyboru miejsca biopsji.
- Elektromiografia (EMG):
- wykazuje cechy uszkodzenia mięśni: krótkie, niskonapięciowe potencjały, wzmożoną aktywność spontaniczną.
- Biopsja mięśnia:
- biopsja mięśnia pozostaje metodą referencyjną w diagnostyce miopatii zapalnych, jednak w praktyce klinicznej jest obecnie wykonywana coraz rzadziej, zarezerwowana jest dla sytuacji diagnostycznie niejednoznacznych lub w celu potwierdzenia rzadkich postaci, takich jak IBM – potwierdza nacieki zapalne, martwicę włókien i cechy regeneracji.
- Diagnostyka onkologiczna:
- w DM, szczególnie u osób >50. r.ż., obowiązkowo należy poszukiwać nowotworu (TK klatki, jamy brzusznej i miednicy, mammografia, kolonoskopia, USG narządów miednicy mniejszej).
Różnicowanie miopatii zapalnych – jak odróżnić od innych przyczyn osłabienia mięśni
Objawy miopatii zapalnych mogą przypominać:
- dystrofie mięśniowe,
- polekowe miopatie (statyny, glikokortykosteroidy, hydroksychlorochina),
- endokrynopatie (niedoczynność tarczycy, zespół Cushinga),
- infekcje wirusowe (HIV, HBV, HCV),
- miastenię.
Prawidłowe różnicowanie ma kluczowe znaczenie, ponieważ leczenie immunosupresyjne w przypadkach wtórnych może pogorszyć przebieg choroby.
Leczenie miopatii zapalnych – glikokortykosteroidy, immunosupresja i nowe terapie
Podstawą terapii są glikokortykosteroidy, często w dużych dawkach (prednizon 0,75–1 mg/kg/dobę). W cięższych przypadkach stosuje się pulsy metyloprednizolonu. Leczenie kontynuuje się do uzyskania remisji, a następnie dawkę redukuje stopniowo przez wiele miesięcy.
W celu ograniczenia toksyczności steroidów i uzyskania lepszej kontroli choroby dołącza się leki immunosupresyjne: metotreksat, azatioprynę, mykofenolan mofetylu lub cyklosporynę. W postaciach opornych stosuje się immunoglobuliny dożylne (IVIG) lub rytuksymab.
W IBM leczenie farmakologiczne ma ograniczoną skuteczność – główną rolę odgrywa rehabilitacja, profilaktyka upadków i leczenie objawowe.
U wszystkich chorych zaleca się fizjoterapię i umiarkowaną aktywność fizyczną, co pomaga utrzymać siłę mięśni i zapobiec przykurczom.
Rokowanie i monitorowanie pacjentów z miopatią zapalną
Rokowanie zależy od postaci choroby i odpowiedzi na leczenie. Najlepsze wyniki osiąga się w DM i PM rozpoznanych wcześnie, natomiast IBM i IMNM mają przebieg przewlekły, często z trwałym deficytem siły.
Czynniki pogarszające rokowanie to:
- późne rozpoznanie,
- obecność przeciwciał anty-SRP,
- zajęcie serca lub płuc (śródmiąższowa choroba płuc),
- współistnienie nowotworu.
Pacjenci wymagają długoterminowej kontroli: monitorowania aktywności CK, funkcji oddechowych i sercowych, a także działań niepożądanych leczenia immunosupresyjnego.
Źródła
- Lundberg, I. E., de Visser, M., & Werth, V. P. (2018). Classification of myositis. Nature Reviews Rheumatology, 14(5), 269–278. https://doi.org/10.1038/nrrheum.2018.41
- Dalakas, M. C. (2015). Inflammatory muscle diseases. The New England Journal of Medicine, 372(18), 1734–1747. https://doi.org/10.1056/NEJMra1402225
- Oddis, C. V., & Aggarwal, R. (2018). Treatment in myositis. Nature Reviews Rheumatology, 14(5), 279–289. https://doi.org/10.1038/nrrheum.2018.37
- Narang, N. S., & Casciola-Rosen, L. (2021). Autoantibodies in idiopathic inflammatory myopathies. Current Opinion in Rheumatology, 33(6), 554–561. https://doi.org/10.1097/BOR.0000000000000835
- EULAR/ACR Classification Criteria for Adult and Juvenile Idiopathic Inflammatory Myopathies. (2017). Annals of the Rheumatic Diseases, 76(12), 1955–1964. https://doi.org/10.1136/annrheumdis-2017-211468