Wyszukaj w publikacjach
Choroba Wilsona – od podwyższonych transaminaz do zaburzeń neuropsychiatrycznych
Choroba Wilsona jest rzadkim, uwarunkowanym genetycznie schorzeniem metabolicznym. Nieleczona prowadzi do postępującego uszkodzenia narządów, niewydolności wątroby i zaburzeń ruchowych, które mogą być nieodwracalne. Wczesne rozpoznanie ma kluczowe znaczenie, ponieważ odpowiednio wcześnie wdrożone leczenie pozwala całkowicie zahamować postęp choroby i zapobiec jej powikłaniom.
Patofizjologia i obraz kliniczny choroby Wilsona
Choroba Wilsona jest wynikiem mutacji w genie ATP7B, zlokalizowanego na chromosomie 13q14.3, który koduje białko odpowiedzialne za transport miedzi w hepatocytach. Defekt tego białka prowadzi do zaburzenia wbudowywania miedzi w ceruloplazminę oraz jej wydzielania z żółcią, czego skutkiem jest toksyczne gromadzenie tego pierwiastka w wątrobie, a następnie w innych narządach, takich jak mózg, nerki, rogówka czy serce. Proces chorobowy przebiega etapowo – od bezobjawowego odkładania miedzi w hepatocytach, przez ich martwicę i uwalnianie miedzi do krwi, aż po wtórne uszkodzenie tkanek. W wątrobie obserwuje się stłuszczenie, zapalenie i włóknienie prowadzące do marskości, natomiast w mózgu dochodzi do uszkodzenia jąder podstawy i móżdżku, z rozplemem gleju astrocytarnego i ubytkami neuronów.
Obraz kliniczny choroby Wilsona jest zróżnicowany i zależy od dominującej lokalizacji zmian. Najczęściej objawy pojawiają się między drugą a trzecią dekadą życia. Postać wątrobowa może obejmować:
- bezobjawowe podwyższenie aminotransferaz,
- zapalenie wątroby,
- marskość,
- piorunującą niewydolność wątroby.
W postaci neurologicznej dominują zaburzenia ruchowe wynikające z uszkodzenia układu pozapiramidowego:
- drżenie,
- dystonia,
- bradykinezja,
- objawy parkinsonowskie,
- ataksja.
Typowe są także:
- zaburzenia mowy,
- ślinotok,
- trudności w połykaniu.
U wielu pacjentów występują zaburzenia psychiatryczne, takie jak:
- zmiany osobowości,
- drażliwość,
- depresja,
- zachowania impulsywne.
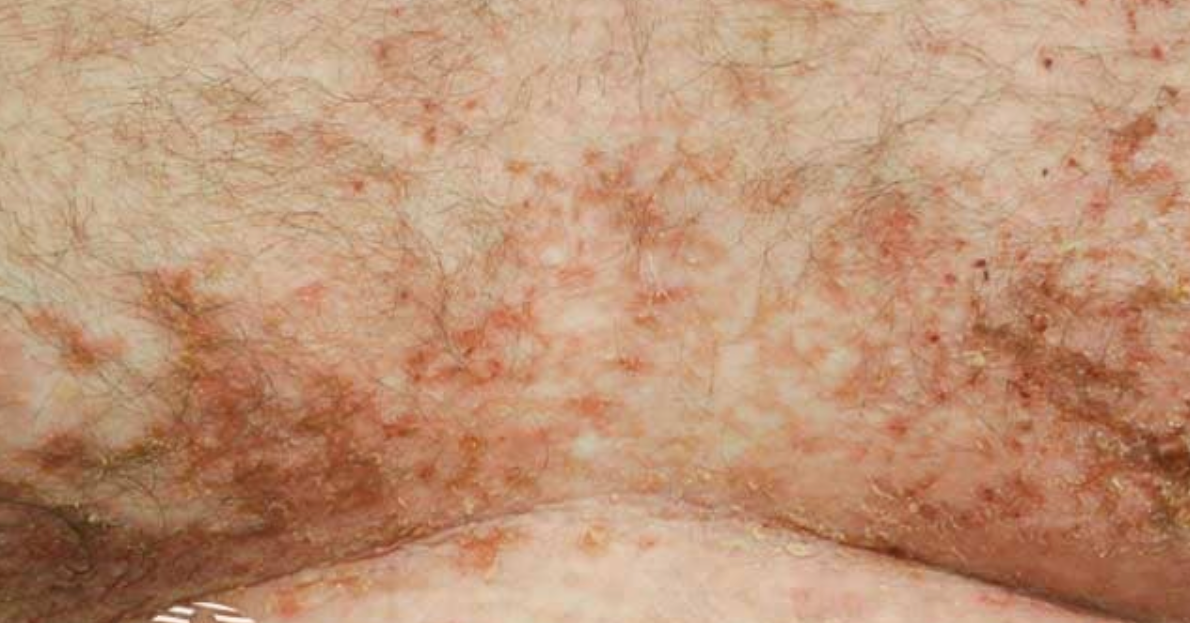
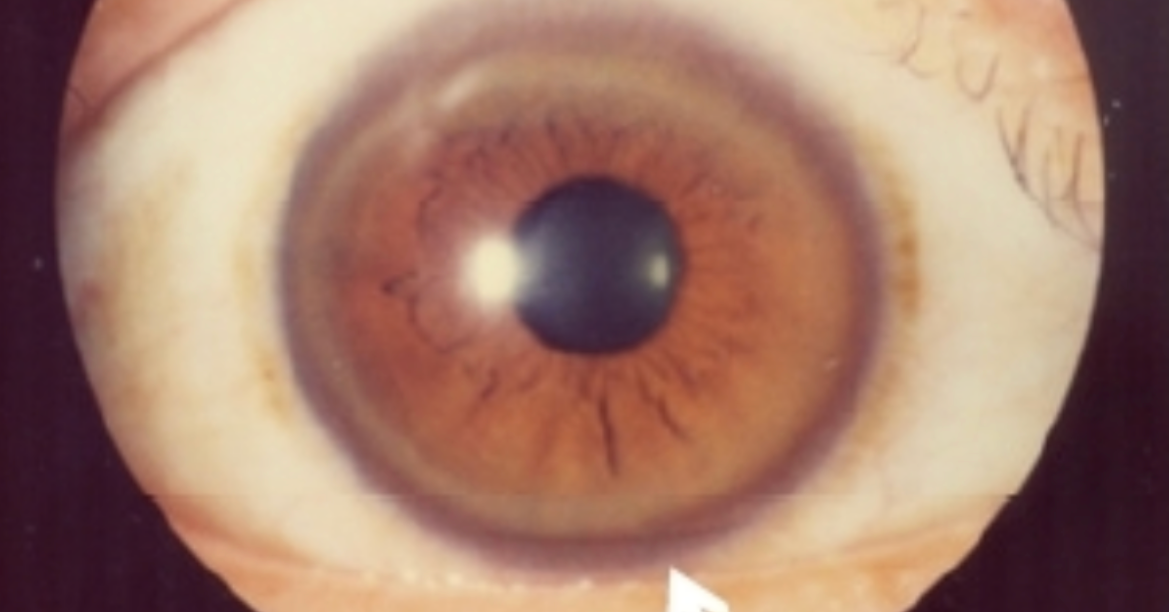
Charakterystycznym objawem okulistycznym jest pierścień Kaysera–Fleischera w rogówce, będący efektem odkładania miedzi.
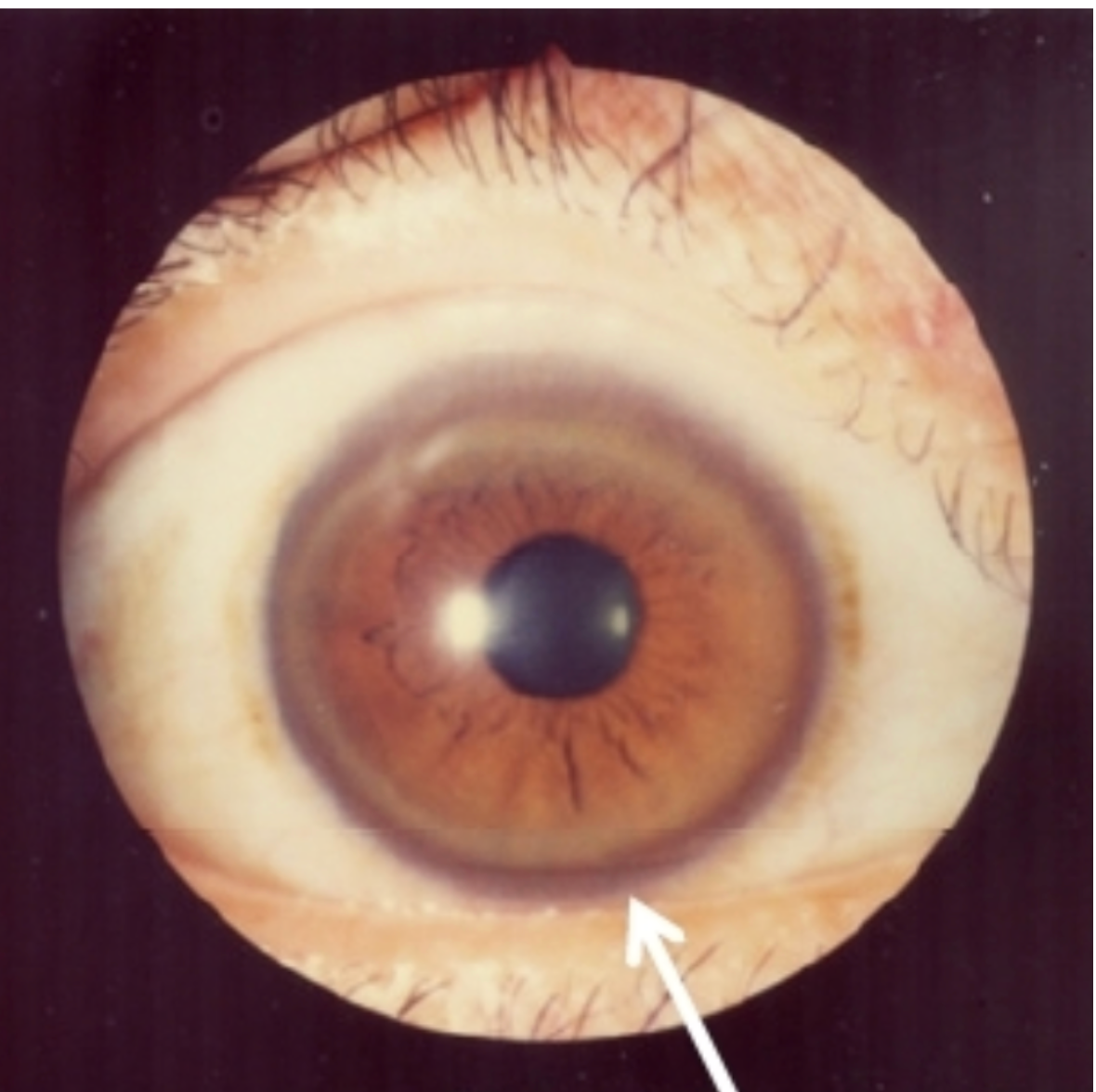
Różnorodność objawów klinicznych i ich stopniowy rozwój sprawiają, że choroba Wilsona stanowi istotne wyzwanie diagnostyczne wymagające czujności i interdyscyplinarnej oceny.
Jak postawić rozpoznanie choroby Wilsona?
Rozpoznanie choroby Wilsona opiera się na zestawieniu:
- objawów klinicznych,
- wyników badań biochemicznych,
- wyników badań obrazowych,
- wyników badań genetycznych.
Pozwala to na potwierdzenie zaburzeń gospodarki miedzią charakterystycznych dla tego schorzenia. Podstawowymi testami diagnostycznymi są oznaczenia:
- stężenia ceruloplazminy i miedzi w surowicy,
- dobowego wydalania miedzi z moczem – które u większości pacjentów jest zwiększone.
Typowo obserwuje się obniżenie stężenia ceruloplazminy oraz miedzi całkowitej, jednak u części chorych z zaawansowanym uszkodzeniem wątroby wartości te mogą pozostawać w normie.
W przypadkach niejednoznacznych pomocne jest oznaczenie zawartości miedzi w bioptacie wątroby lub badanie mutacji w genie ATP7B, których obecność potwierdza rozpoznanie.
U pacjentów z objawami neurologicznymi kluczowe znaczenie ma badanie okulistyczne w lampie szczelinowej w celu wykrycia pierścienia Kaysera–Fleischera oraz MR mózgu, w którym typowo stwierdza się zmiany w jądrach podstawy, wzgórzach i móżdżku.
Dodatkowo, w ocenie prawdopodobieństwa rozpoznania stosuje się system punktowy Ferenciego, uwzględniający:
- wyniki badań laboratoryjnych,
- obecność objawów neurologicznych,
- obecność pierścienia rogówkowego
- obecność mutacji genetycznych.
W przypadku stwierdzenia choroby u jednego z członków rodziny konieczne jest również badanie krewnych pierwszego stopnia, co umożliwia wczesne wykrycie postaci bezobjawowych i szybkie wdrożenie leczenia.
Leczenie – jak postępować przy mutacji ATP7B?
Po rozpoznaniu choroby Wilsona konieczne jest natychmiastowe wdrożenie leczenia mającego na celu usunięcie nadmiaru miedzi z organizmu oraz zapobieganie jej ponownemu odkładaniu się w tkankach.
Podstawę terapii stanowią leki chelatujące miedź, takie jak d-penicylamina i trientyna, które zwiększają jej wydalanie z moczem. Leczenie rozpoczyna się od małych dawek, stopniowo je zwiększając, aby uniknąć nagłego uwalniania miedzi z tkanek i pogorszenia stanu neurologicznego. Równocześnie zaleca się suplementację pirydoksyny (witaminy B6), niezbędnej przy stosowaniu d-penicylaminy.
Alternatywą lub leczeniem podtrzymującym są preparaty cynku, które hamują wchłanianie miedzi z przewodu pokarmowego poprzez indukcję metalotioneiny w enterocytach. Cynk jest szczególnie polecany u pacjentów bezobjawowych, w postaciach przedklinicznych oraz u dzieci i kobiet w ciąży.
W trakcie terapii niezbędne jest regularne monitorowanie:
- wydalania miedzi z moczem,
- parametrów wątrobowych,
- morfologii krwi obwodowej.
Istotna jest również ścisła kontrola kliniczna, ponieważ nawet krótkotrwałe przerwanie leczenia może prowadzić do nawrotu objawów i nieodwracalnego uszkodzenia narządów.
W przypadku nieskuteczności lub nietolerancji leczenia farmakologicznego, a także w sytuacjach piorunującej niewydolności wątroby, rozważa się przeszczepienie wątroby, które koryguje defekt metaboliczny i przywraca prawidłową gospodarkę miedzi. Leczenie choroby Wilsona jest długotrwałe i wymaga ścisłej współpracy pacjenta z zespołem specjalistów, co pozwala utrzymać prawidłową funkcję narządów i zapobiec progresji choroby.
Rokowanie u pacjentów z zaburzeniem gospodarki miedzią
Rokowanie w chorobie Wilsona w dużej mierze zależy od:
- momentu rozpoznania,
- skuteczności wdrożonego leczenia.
W przypadkach, gdy choroba zostaje wykryta we wczesnym stadium i szybko rozpoczyna się terapię chelatującą lub cynkową, możliwe jest pełne zahamowanie postępu choroby oraz zachowanie prawidłowej funkcji wątroby i ośrodkowego układu nerwowego. Pacjenci dobrze reagujący na leczenie mogą prowadzić normalne życie przy zachowaniu regularnych kontroli i przestrzeganiu zaleceń terapeutycznych. W postaciach zaawansowanych, zwłaszcza z rozległym uszkodzeniem wątroby lub ciężkimi objawami neurologicznymi, rokowanie jest mniej korzystne, a skuteczność leczenia ograniczona. U części chorych, mimo stosowania odpowiedniej farmakoterapii, dochodzi do nieodwracalnych zmian neurologicznych lub rozwoju marskości wątroby. Najczęstszą przyczyną pogorszenia rokowania jest nieregularne przyjmowanie leków lub przerwanie terapii, co prowadzi do nawrotu objawów i progresji choroby.
Źródła
- Weiss, K. H., & Schilsky, M. (2023). Wilson Disease. GeneReviews® - NCBI Bookshelf. https://www.ncbi.nlm.nih.gov/books/NBK1512/
- Tarnacka, B., & Członkowska, A. (2008). Choroba Wilsona. Polski Przegląd Neurologiczny, 4(3), 125–128. https://doi.org/10.5603/ppn.20068
- Choroba Wilsona u dzieci – wytyczne diagnostyki i leczenia. Aktualne stanowisko ESPGHAN - Standardy Medyczne. https://www.standardy.pl/artykuly/id/1564

![PKwPOZ_Gastroenterologia_Choroba_Wilsona_co_trzeba_wiedzieć[jesień2025]](https://cdn.remedium.md/image/video_thumbnail/2025/11/27/09/prof-dr-hab-n-med-piotr-socha-png-69280d8e3bdb4.png)