Wyszukaj w poradnikach
Celiakia
Krótka teoria
Celiakia to autoimmunologiczna enteropatia wywoływana przez gluten u osób z predyspozycją genetyczną (HLA-DQ2.5 lub DQ8). Kluczową rolę odgrywa transglutaminaza tkankowa 2 (tTG), która modyfikuje peptydy gliadyny, prowadząc do ich prezentacji przez APC i aktywacji odpowiedzi limfocytarnej. Efektem jest zanik kosmków jelitowych i naciek limfocytów, klasyfikowany wg skali Marsh.
Wyróżnia się postacie:
- klasyczną,
- nieklasyczną,
- bezobjawową,
- potencjalną,
- oporną na leczenie.
Celiakia wiąże się z ryzykiem osteoporozy, niepłodności, a w skrajnych przypadkach – chłoniaka T-komórkowego jelita cienkiego.
Wywiad
- Czy występują objawy ze strony przewodu pokarmowego, takie jak przewlekłe lub nawracające biegunki, bóle brzucha, wzdęcia, zaparcia lub uczucie przelewania? – objawy jelitowe są typowe w klasycznej postaci celiakii, ale mogą być łagodne lub nieobecne, zwłaszcza u dorosłych.
- Czy pojawia się znaczna utrata masy ciała, brak apetytu lub nietolerancja pieczywa i produktów zbożowych? – zespół złego wchłaniania i nieświadoma eliminacja glutenu mogą prowadzić do samoistnych ograniczeń dietetycznych.
- Czy występują objawy ogólne: przewlekłe zmęczenie, bóle głowy, trudności z koncentracją, zawroty głowy, bladość skóry, łamliwość włosów? – mogą wskazywać na niedobory żelaza, witaminy B12 lub kwasu foliowego – częste u pacjentów z celiakią.
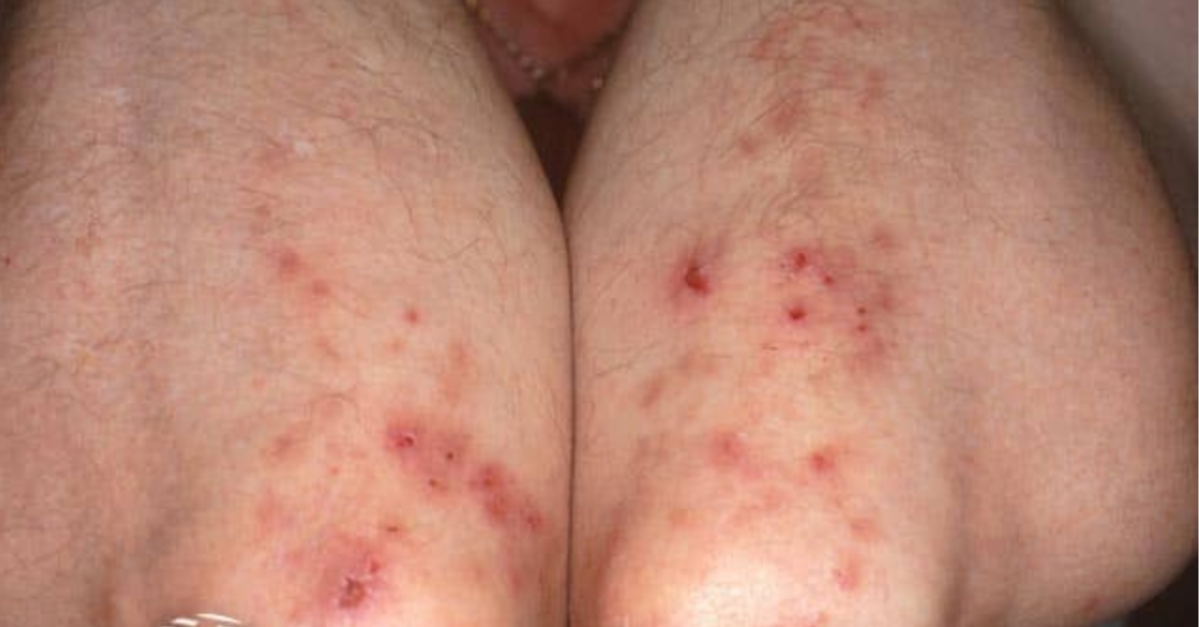
- Czy występują swędzące zmiany skórne – pęcherzykowe, zlokalizowane na łokciach, kolanach, karku, pośladkach? – to może być dermatitis herpetiformis – skórna postać celiakii, często nierozpoznawana.
- Czy kiedykolwiek występowały problemy z płodnością, poronienia, zaburzenia miesiączkowania lub spadek libido? – objawy ginekologiczne i andrologiczne mogą być jedyną manifestacją choroby.
- Czy w rodzinie występują choroby autoimmunologiczne – celiakia, cukrzyca typu 1, choroba Hashimoto, łuszczyca, zapalenia stawów? – wywiad rodzinny zwiększa prawdopodobieństwo choroby – predyspozycje genetyczne mają kluczowe znaczenie.
- Czy w przeszłości wykonywano badania w kierunku celiakii – przeciwciała (np. anty-tTG, EMA), gastroskopię z biopsją jelita cienkiego? Czy była stosowana dieta bezglutenowa, nawet próbnie? – rozpoczęcie diety bez wcześniejszej diagnostyki może prowadzić do fałszywie ujemnych wyników.
- Czy u dzieci występowały problemy ze wzrastaniem, opóźnione dojrzewanie lub niska masa ciała? – u pacjentów pediatrycznych to częsta, nierzadko jedyna manifestacja celiakii.
- Jak wygląda codzienna dieta – czy pacjent spożywa regularnie pieczywo, makaron, kasze, płatki? Czy czyta etykiety produktów, czy występują trudności w unikaniu glutenu poza domem? – ocena rzeczywistego narażenia na gluten jest kluczowa – błędy dietetyczne są częste nawet u pacjentów z rozpoznaniem.
- Jakie leki pacjent stosuje przewlekle? Czy występują inne choroby – np. tarczycy, cukrzyca, choroby skóry, zapalenia stawów? – celiakia często współistnieje z innymi chorobami autoimmunologicznymi.
- Czy pojawiają się bóle kości, złamania przy niewielkich urazach, skurcze mięśni, obniżenie wzrostu (u dzieci)? – zmiany metaboliczne kości są częstym powikłaniem związanym z zaburzeniami wchłaniania.
- Czy występują objawy depresyjne – przewlekły spadek nastroju, brak motywacji, lęk? – objawy psychiczne mogą być zarówno skutkiem niedoborów, jak i przewlekłego stanu zapalnego.
- Czy wcześniej rozpoznano zespół jelita drażliwego, ale leczenie nie przyniosło poprawy? – u części pacjentów z celiakią początkowo stawiana jest błędna diagnoza IBS.
Ocena kliniczna
- Stan ogólny pacjenta:
- pomiar temperatury: w przebiegu celiakii nie obserwuje się typowo gorączek, jednak stan podgorączkowy może towarzyszyć wtórnym infekcjom, np. zakażeniom dróg moczowych lub infekcjom górnych dróg oddechowych u dzieci z niedoborem odporności;
- ocena stanu odżywienia, ubytku masy ciała, BMI: warto zanotować, czy pacjent mieści się w przedziale <18,5 kg/m2 – u dorosłych może to sugerować przewlekłe zaburzenia wchłaniania;
- pomiar wysokości ciała (dzieci): ubytek wysokości ciała u osób dorosłych nie jest typowy, natomiast u dzieci należy zwrócić szczególną uwagę na spowolnienie tempa wzrastania i opóźnienie dojrzewania płciowego; warto sięgnąć po siatki centylowe i ocenić trend w czasie;
- oznaki anemizacji: bladość skóry i spojówek, tachykardia, uczucie duszności wysiłkowej, łamliwość paznokci – objawy te mogą sugerować niedobór żelaza lub B12.
- Ocena sprawności funkcjonalnej:
- u pacjentów w starszym wieku lub z podejrzeniem powikłań kostnych warto ocenić ogólną sprawność i ryzyko upadków, np. za pomocą testu „wstań i idź”;
- wynik >14 s może wskazywać na osłabienie mięśniowe i ryzyko upadków – w celiakii często wtórne do niedoborów witaminy D i zaburzeń metabolicznych kości.
- Badanie internistyczne:
- skóra i błony śluzowe: bladość, suchość, zmiany troficzne, obecność aft i nadżerek;
- palpacja brzucha: wzdęcie, przelewania, tkliwość w okolicy pętli jelitowych – objawy nieswoiste, ale mogą towarzyszyć celiakii klasycznej;
- ocena węzłów chłonnych: powiększenie nie jest typowe w celiakii, ale może występować wtórnie, np. w przebiegu infekcji wirusowych (EBV, CMV) lub współistniejących chorób autoimmunologicznych.
- Skrócone badanie neurologiczne:
- ocena siły mięśniowej i napięcia: niedobory witaminy D i B12 mogą prowadzić do osłabienia siły mięśniowej, szczególnie w obrębie kończyn dolnych;
- ocena czucia: parestezje, drętwienia, zaburzenia propriocepcji mogą świadczyć o neuropatii obwodowej, wtórnej do niedoborów (B12, miedź);
- badanie równowagi i chodu: zaburzenia równowagi mogą pojawić się u pacjentów z ataksją glutenozależną (neuroceliakią), choć są stosunkowo rzadkie.
- Ocena skóry:
- wysypka o charakterze grudkowo-pęcherzykowym, symetryczna, zlokalizowana na łokciach, pośladkach, kolanach, karku – sugeruje dermatitis herpetiformis;
- wskazana konsultacja dermatologiczna i ewentualne pobranie wycinka do badania immunopatologicznego (wykazanie złogów IgA w brodawkach skórnych).
Kryteria rozpoznania i badania dodatkowe
Rozpoznanie celiakii opiera się na wynikach badań serologicznych i/lub histopatologicznych, w połączeniu z obrazem klinicznym i wywiadem. Kluczowe jest, aby diagnostykę prowadzić przed wprowadzeniem diety bezglutenowej – eliminacja glutenu przed badaniami może skutkować fałszywie ujemnymi wynikami. Diagnostyka celiakii nie należy do świadczeń gwarantowanych w POZ – pacjent powinien zostać skierowany do poradni gastroenterologicznej lub wykonać badania serologiczne odpłatnie.
- Badania serologiczne – pierwsza linia diagnostyczna:
- przeciwciała anty-tTG w klasie IgA,
- całkowite stężenie IgA (u osób z niedoborem IgA wyniki anty-tTG mogą być fałszywie ujemne),
- jeśli występuje niedobór IgA: przeciwciała w klasie IgG (DGP lub EMA);
- badania należy wykonywać przy założeniu obecności glutenu w diecie przez co najmniej 6 tygodni.
- Biopsja dwunastnicy – wskazana w większości przypadków u dorosłych:
- wskazania obejmują:
- dodatnie przeciwciała anty-tTG <10× ULN,
- wątpliwy obraz kliniczny,
- niespójności między serologią a objawami,
- współistnienie innych chorób,
- brak poprawy mimo GFD,
- pobiera się co najmniej 4 wycinki z części dystalnej dwunastnicy oraz ≥1 z opuszki,
- histopatologię ocenia się wg klasyfikacji Marsh-Oberhuber.
- wskazania obejmują:
- Diagnostyka bez biopsji – możliwa u dzieci:
- TGA-IgA ≥10× ULN w dwóch niezależnych próbkach + dodatni EMA-IgA w drugiej próbce,
- uzupełniająco: wykluczenie niedoboru IgA i potwierdzenie spożywania glutenu.
Algorytm diagnostyczny bez biopsji został potwierdzony jako bezpieczny jedynie w populacji dziecięcej. U osób dorosłych nadal rekomenduje się wykonanie biopsji dwunastnicy – nawet przy wysokich wartościach przeciwciał tTG-IgA, ze względu na wyższe ryzyko chorób współistniejących oraz trudności diagnostyczne w tej grupie wiekowej.
- Badania dodatkowe i uzupełniające (ocena stanu ogólnego):
- morfologia krwi obwodowej,
- ferrytyna, żelazo, wit. B12, kwas foliowy, wit. D (niedostępne w POZ), wapń, fosfor (niedostępne w POZ), albumina,
- TSH, fT4,
- próby wątrobowe,
- glukoza na czczo,
- u dzieci: ocena wzrastania, ewentualnie radiologiczna ocena wieku kostnego,
- do rozważenia: badanie densytometryczne (DEXA) – zarezerwowane dla pacjentów z klinicznymi cechami osteoporozy, złamaniami lub długotrwałym niedożywieniem;
U niektórych pacjentów z celiakią obserwuje się gorszą odpowiedź immunologiczną na szczepienie przeciwko HBV. Warto oznaczyć poziom przeciwciał anty-HBs (niedostępne w POZ) u osób szczepionych w dzieciństwie – w razie braku odpowiedzi można rozważyć doszczepienie. Dotyczy to zwłaszcza pacjentów z niedoborami odporności lub nieprawidłową odpowiedzią immunologiczną na inne szczepienia.
Diagnostyka różnicowa powinna uwzględniać m.in.:
- IBS,
- nietolerancję laktozy lub fruktozy,
- SIBO,
- infekcje pasożytnicze,
- chorobę Leśniowskiego–Crohna,
- niedobory enzymatyczne,
- chłoniaki jelita cienkiego.
Uwaga! Czerwona flaga!
Pojawienie się poniższych objawów lub zespołów objawów powinno skłonić do pilnej weryfikacji rozpoznania lub rozszerzenia diagnostyki różnicowej, ponieważ mogą wskazywać na inne, poważniejsze jednostki chorobowe, współistniejące zaburzenia lub powikłania zaawansowanej, nieleczonej celiakii:
- niedokrwistość oporna na suplementację, mimo stosowania diety bezglutenowej i braku potwierdzonej utraty krwi – może sugerować nowotwory przewodu pokarmowego (np. chłoniaka T-komórkowego jelita cienkiego, EATL);
- nawracające bóle brzucha z objawami niedrożności lub wyraźną utratą masy ciała – konieczne różnicowanie z chłoniakiem, chorobą Crohna, rakiem jelita cienkiego;
- wysoka męczliwość, duszność spoczynkowa, tachykardia, ortostatyczne spadki ciśnienia tętniczego – mogą świadczyć o ciężkiej anemii lub odwodnieniu w przebiegu enteropatii z masywną utratą elektrolitów;
- nagłe osłabienie siły mięśniowej, zaburzenia czucia, zaburzenia chodu lub równowagi – podejrzenie neuropatii obwodowej, neuroceliakii lub niedoboru B12; konieczne pilne różnicowanie z ostrym zespołem neurologicznym (np. GBS);
- utrata przytomności, drgawki, zaburzenia świadomości – hipoglikemia, encefalopatia z niedoboru witamin (B1, B6), majaczenie – wymagają pilnej interwencji;
- biegunka z domieszką krwi, gorączką i leukocytozą – przemawia przeciwko celiakii jako jedynej przyczynie objawów, sugeruje infekcję lub IBD;
- szybkie pogorszenie stanu ogólnego u dziecka z objawami zespołu złego wchłaniania – może świadczyć o tzw. przełomie celiakalnym (celiac crisis) – rzadki, ale potencjalnie zagrażający życiu stan u dzieci.
W przypadku wystąpienia któregokolwiek z powyższych objawów należy rozważyć skierowanie do szpitala lub pilnej konsultacji specjalistycznej (gastroenterologicznej, neurologicznej, hematologicznej, onkologicznej).
Leczenie i postępowanie
Podstawą leczenia celiakii jest ścisła dieta bezglutenowa (GFD), która prowadzi do ustąpienia objawów klinicznych, normalizacji przeciwciał i regeneracji śluzówki jelita cienkiego. Nawet niewielkie odstępstwa od diety mogą prowadzić do nawrotu objawów i ryzyka powikłań.
- Wdrożenie leczenia dietetycznego wymaga edukacji pacjenta i jego otoczenia. Warto zapewnić wsparcie dietetyka przeszkolonego w zakresie GFD, przekazać pacjentowi materiały edukacyjne oraz wskazać wiarygodne źródła (np. aplikacje mobilne, certyfikowane poradniki żywieniowe).
- Konieczna jest suplementacja niedoborów stwierdzonych w badaniach laboratoryjnych. Najczęściej dotyczy to:
- żelaza (z lub bez niedokrwistości),
- kwasu foliowego, witaminy B12, witaminy D,
- wapnia – szczególnie u osób z osteopenią lub niskim spożyciem produktów mlecznych.
- Ocena skuteczności leczenia obejmuje obserwację kliniczną, ocenę serologii oraz stanu odżywienia.
- Przeciwciała tTG (lub DGP – w przypadku niedoboru IgA) powinny stopniowo spadać i ulec normalizacji w ciągu 12–24 miesięcy.
- Brak poprawy klinicznej lub utrzymywanie się wysokich poziomów przeciwciał może wskazywać na błędy dietetyczne, nieświadome spożycie glutenu lub współistnienie innych chorób.
- W razie podejrzenia celiakii opornej na leczenie należy rozważyć dalszą diagnostykę: (re)biopsję, testy serologiczne w kierunku innych enteropatii oraz konsultację specjalistyczną. Refrakcyjna postać celiakii u dzieci jest skrajnie rzadka – konieczne jest wykluczenie innych przyczyn objawów, np. choroby Crohna, niedoborów enzymatycznych, alergii pokarmowych.
- Dieta bezglutenowa wiąże się z dużym obciążeniem emocjonalnym i społecznym – szczególnie u młodzieży i młodych dorosłych. Warto zadbać o wsparcie psychologiczne, grupy wsparcia lub konsultację psychiatryczną w przypadku depresji, zaburzeń odżywiania lub obniżonej jakości życia.
Przykładowa wizyta
Wywiad
Do gabinetu POZ zgłasza się 23-letnia pacjentka z przewlekłym uczuciem zmęczenia, wzdęciami i nieregularnymi wypróżnieniami. Od kilku miesięcy obserwuje nawracające bóle brzucha i spadek masy ciała o ok. 5 kg, mimo braku zmiany diety. W wywiadzie przewlekła niedokrwistość z niskim poziomem ferrytyny, pomimo wcześniejszej suplementacji żelazem. W dzieciństwie leczona z powodu alergii pokarmowej, obecnie zdrowa, nie stosuje leków. Nieprawidłowości w miesiączkowaniu – cykle nieregularne, co 40–50 dni. Matka pacjentki choruje na chorobę Hashimoto. Pacjentka wspomina, że próbowała diety bezglutenowej, „bo czuła się wtedy lepiej”.
Badanie przedmiotowe
Stan ogólny dobry, BMI 19,1 kg/m2. Skóra blada, suche łokcie, pojedyncze zmiany grudkowe na powierzchni prostowników przedramion. Język gładki, czerwony, z widocznymi pęknięciami. Brzuch miękki, niebolesny, nieznaczne przelewania w lewym podbrzuszu. Objaw Goldflama ujemny obustronnie. Osłuchowo bez zmian. W badaniu neurologicznym nie stwierdza się deficytów. Test „wstań i idź”: 11 sekund – samodzielna, sprawna w czynnościach dnia codziennego.
Zalecenia i diagnostyka
Zlecono badania: morfologię, ferrytynę, stężenie witaminy B12, kwasu foliowego, TSH, fT4, glukozę na czczo, przeciwciała anty-tTG w klasie IgA oraz całkowite stężenie IgA (badania te pacjentka wykona odpłatnie). W razie niedoboru IgA – oznaczenie przeciwciał w klasie IgG (DGP). Zalecono kontynuację diety zawierającej gluten do czasu uzyskania wyników.
Dalsze postępowanie
Omówiono z pacjentką podejrzenie celiakii. W zależności od wyników serologii – planowane skierowanie na gastroskopię z biopsją dwunastnicy. Zalecono unikanie diety eliminacyjnej do czasu zakończenia diagnostyki. Przekazano broszurę edukacyjną dotyczącą celiakii i omówiono potencjalne objawy alarmowe.
Wizyta kontrolna
Omówienie wyników badań
W badaniach laboratoryjnych stwierdzono:
- hemoglobina 11,0 g/dl, MCV 74 fl, ferrytyna 8 ng/mL – niedokrwistość mikrocytarna z niedoboru żelaza,
- poziom witaminy D – 14 ng/ml (niedobór),
- TSH i fT4 w normie,
- IgA w normie, przeciwciała anty-tTG IgA dodatnie, w miano przekraczającym 12× ULN. W drugim oznaczeniu potwierdzono wynik dodatni oraz obecność przeciwciał EMA w klasie IgA.
Na podstawie wywiadu, obrazu klinicznego i wyników badań – spełniono kryteria rozpoznania celiakii. Pacjentka spełnia przesłanki do postawienia rozpoznania bez konieczności biopsji jelita cienkiego, zgodnie z kryteriami ESPGHAN (≥10× ULN + EMA w osobnej próbce + objawy kliniczne).
Zalecenia i leczenie
Wprowadzono dożywotnią dietę bezglutenową, omówiono dokładnie źródła glutenu i potencjalne pułapki żywieniowe (m.in. gluten w lekach, kosmetykach, sosach). Wydano skierowanie na konsultację z dietetykiem specjalizującym się w celiakii. Zalecono suplementację: żelazo (dwusiarczan żelaza – 100 mg dziennie, do kontroli parametrów po 3 miesiącach) oraz witaminę D – 2000 IU dziennie przez 3 miesiące, następnie rewaluacja. Omówiono konieczność regularnych kontroli – pierwsza wizyta kontrolna za 6 miesięcy z oznaczeniem anty-tTG, morfologii krwi obwodowej i ferrytyny. Przekazano pacjentce materiały edukacyjne nt. życia z celiakią oraz listę certyfikowanych produktów i aplikacji mobilnych wspierających prowadzenie GFD. Wskazano lokalne grupy wsparcia oraz możliwość udziału w programie edukacyjnym prowadzonym przez organizację pacjencką.
Kody ICD-10
Choroby układu pokarmowego
Referencje
- Gajewski, P. (2024). Interna Szczeklika 2024/25. Mały podręcznik. Kraków: Medycyna Praktyczna.
- Husby, S., Koletzko, S., Korponay-Szabó, I. R., Mearin, M. L., Phillips, A., Shamir, R., ... & Szajewska, H. (2020). European Society Paediatric Gastroenterology, Hepatology and Nutrition guidelines for diagnosing coeliac disease 2020. Journal of Pediatric Gastroenterology and Nutrition, 70(1), 141–156.
- Mearin, M. L., Koletzko, S., Auricchio, R., Catassi, C., Castro, M., Giersiepen, K., ... & Szajewska, H. (2022). ESPGHAN position paper on management and follow-up of children and adolescents with coeliac disease. Journal of Pediatric Gastroenterology and Nutrition, 75(2), 171–194.
- Lebwohl, B., Sanders, D. S., & Green, P. H. R. (2018). Coeliac disease. The Lancet, 399(10344), 2413–2426. https://doi.org/10.1016/S0140-6736(22)00794-2
- Rubio-Tapia, A., Hill, I. D., Kelly, C. P., Calderwood, A. H., & Murray, J. A. (2013). ACG clinical guidelines: diagnosis and management of celiac disease. American Journal of Gastroenterology, 108(5), 656–676.
- Mearin, M. L., Szajewska, H., & Papadopoulou, A. (2022). New guidelines for the diagnosis of paediatric coeliac disease – ESPGHAN Advice Guide. European Society for Paediatric Gastroenterology, Hepatology and Nutrition.
![PKwPOZ_Gastroenterologia_Celiakia_a_może_coś_jeszcze?[jesień2025]](https://cdn.remedium.md/image/video_thumbnail/2025/11/27/09/prof-dr-hab-n-med-michal-kukla-png-69280dda3d091.png)



![PKwPOZ_Gastroenterologia_Sesja_3_panel_dyskusyjny[jesień2025]](https://cdn.remedium.md/image/video_thumbnail/2025/11/27/13/3-png-69283f5a852e7.png)

![PKwPOZ_Gastroenterologia_Wszystko_o_uchyłkach[jesień2025]](https://cdn.remedium.md/image/video_thumbnail/2025/11/27/09/dr-n-med-anna-pietrzak-png-692807b13b90d.png)