Wyszukaj w publikacjach
Hipotonia, wymioty i drgawki u niemowlęcia – co trzeba wiedzieć o wrodzonych wadach metabolizmu?

Wrodzone wady metabolizmu stanowią niezwykle zróżnicowaną grupę rzadkich chorób monogenowych. Choć poszczególne jednostki chorobowe występują z niską częstością, ich łączna częstość sprawia, że w praktyce klinicznej stanowią istotne wyzwanie diagnostyczne i terapeutyczne.
Patofizjologia i obraz kliniczny wrodzonych wad metabolizmu
Patofizjologia wrodzonych wad metabolizmu opiera się na defekcie genetycznym prowadzącym do zaburzenia funkcji:
- enzymów,
- białek transportowych,
- struktur organellowych.
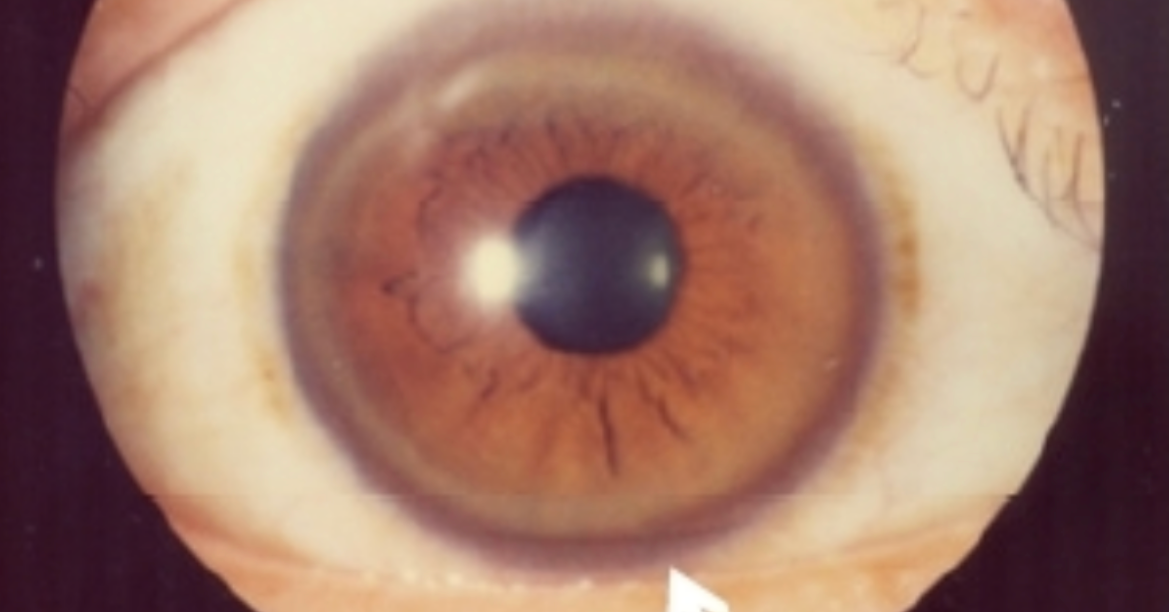
Do takich chorób należą m.in.: fenyloketonuria, mukopolisacharydozy, galaktozemia, choroba Pompego, choroba Wilsona.
Zaburzenia tych funkcji skutkują zakłóceniem kluczowych szlaków biochemicznych. Mechanizmy mogą obejmować:
- akumulację toksycznych metabolitów powyżej miejsca bloku metabolicznego – np. w defektach cyklu mocznikowego;
- niedobór energii wynikający z upośledzenia glikolizy, glukoneogenezy czy utleniania kwasów tłuszczowych;
- przewlekłe gromadzenie nieprawidłowych makrocząsteczek w lizosomach i peroksysomach.
Obraz kliniczny jest równie zróżnicowany jak podłoże molekularne – od ostrych, szybko postępujących stanów zagrożenia życia u noworodków, przez epizody metabolicznej dekompensacji w dzieciństwie, po przewlekłe i wielonarządowe manifestacje w wieku dorosłym.
W okresie noworodkowym dominują objawy nieswoiste:
W późniejszym wieku kliniczna prezentacja obejmuje:
- nawracające epizody hipoglikemii,
- niewydolność wątroby i serca,
- objawy neurologiczne – drgawki, opóźnienie rozwoju, regres umiejętności,
- cechy dysmorfii i przewlekłej choroby wielonarządowej charakterystyczne dla chorób spichrzeniowych.
Tak szeroki wachlarz manifestacji klinicznych wymaga wysokiego stopnia czujności diagnostycznej, gdyż wczesne rozpoznanie i wdrożenie leczenia może decydować o rokowaniu i jakości życia pacjentów.
Kiedy podejrzewać wrodzone wady metabolizmu?
Wrodzone wady metabolizmu należy podejrzewać u noworodków i dzieci, u których pojawiają się niespecyficzne, ale ciężkie objawy kliniczne niewyjaśnione innymi częstszymi przyczynami. Szczególnie alarmujące są przypadki:
- encefalopatii,
- napadów drgawkowych,
- hipotonii,
- zaburzeń karmienia,
- uporczywych wymiotów,
- śpiączki,
- niewydolności wielonarządowej występujące po krótkim okresie pozornego zdrowia.
Podejrzenie powinno nasuwać także nagłe pogorszenie stanu klinicznego po infekcji, zmianie diety, głodzeniu nocnym czy innym stanie nasilonego katabolizmu, a także brak odpowiedzi na standardowe leczenie sepsy lub encefalopatii niedotlenieniowo-niedokrwiennej.
W obrazie laboratoryjnym na podejrzenie wrodzonej wady metabolizmu wskazują m.in.:
- hipoglikemia,
- kwasica metaboliczna z podwyższoną luką anionową,
- hiperamonemia,
- hiperlaktatemia,
- obecność charakterystycznych metabolitów w moczu lub osoczu.
Istotne znaczenie ma także wywiad rodzinny, obejmujący niewyjaśnione zgony noworodków czy choroby wieku dziecięcego.
Z uwagi na nieswoistość objawów, każdy noworodek w ciężkim stanie, zwłaszcza z dominującymi objawami neurologicznymi i zaburzeniami metabolicznymi, powinien być oceniany pod kątem możliwej wrodzonej wady metabolizmu.
Jak postawić rozpoznanie wrodzonej wady metabolizmu?
Rozpoznanie wrodzonej wady metabolizmu wymaga zintegrowanego podejścia klinicznego, biochemicznego i genetycznego. Kluczowe znaczenie ma wstępna ocena noworodka lub dziecka z nieswoistymi, ale ciężkimi objawami. Podstawowe badania obejmują:
- morfologię krwi obwodowej,
- gazometrię,
- glikemię,
- stężenia mleczanów,
- stężenie amoniaku,
- aktywność aminotransferaz,
- aktywność kinazy kreatynowej,
- profil aminokwasów i kwasów organicznych w osoczu i moczu.
Badania genetyczne, w tym sekwencjonowanie nowej generacji, stanowią podstawę potwierdzenia diagnozy i umożliwiają poradnictwo rodzinne.
W praktyce klinicznej najważniejsze jest szybkie rozpoznanie sytuacji potencjalnie odwracalnej i wdrożenie działań terapeutycznych jeszcze przed uzyskaniem pełnego potwierdzenia laboratoryjnego, co może decydować o rokowaniu i ograniczeniu ciężkich następstw neurologicznych.
Leczenie – jak postępować po rozpoznaniu WWM?
Leczenie wrodzonych wad metabolizmu wymaga natychmiastowego działania i ukierunkowanego postępowania, które ma na celu:
- stabilizację pacjenta,
- ograniczenie skutków dekompensacji metabolicznej,
- zapobieganie dalszej akumulacji toksycznych metabolitów.
W pierwszej kolejności stosuje się resuscytację zgodnie z zasadami intensywnej terapii oraz wprowadza żywienie dożylne z podażą glukozy, aby zahamować katabolizm i zapewnić podstawowe źródło energii.
U pacjentów z hiperamonemią wdraża się leki wiążące azot (benzoesan sodu oraz fenylomaślan sodu – 250 mg/kg m.c./dobę, maksymalnie 12 g/dobę), a w ciężkich przypadkach konieczne jest zastosowanie dializoterapii.
Leczenie specyficzne zależy od rodzaju defektu metabolicznego i może obejmować:
- stosowanie diet eliminacyjnych (np. niskobiałkowych, z ograniczeniem tłuszczów lub cukrów prostych),
- suplementację brakujących enzymów, koenzymów lub witamin (np. pirydoksyny, biotyny, tiaminy),
- terapie usuwające toksyny z krążenia.
Równolegle niezwykle istotne są działania wspomagające – intensywne nawadnianie, korekta zaburzeń elektrolitowych i równowagi kwasowo-zasadowej, leczenie drgawek oraz profilaktyka powikłań neurologicznych i wielonarządowych.
Kluczowe znaczenie ma współpraca interdyscyplinarnego zespołu, co umożliwia nie tylko opanowanie ostrego kryzysu, ale także wdrożenie długoterminowej terapii zapobiegającej nawrotom i poprawiającej rokowanie chorego.
Rokowanie w pediatrii metabolicznej
Rokowanie w wrodzonych wadach metabolizmu zależy od rodzaju defektu, ciężkości objawów oraz szybkości rozpoznania i leczenia. W chorobach ujawniających się w okresie noworodkowym bez szybkiej interwencji jest ono zwykle niekorzystne, a śmiertelność wysoka. Wczesne wdrożenie terapii poprawia przeżywalność, choć często pozostają następstwa neurologiczne. Lepsze rokowanie dotyczy schorzeń możliwych do kontrolowania dietą lub farmakoterapią, natomiast choroby o przebiegu postępującym, z neurodegeneracją czy niewydolnością wielonarządową, wiążą się z poważnym ryzykiem złego wyniku.
Źródła
- Jeanmonod, R., Asuka, E., & Jeanmonod, D. (2023). Inborn errors of metabolism. StatPearls - NCBI Bookshelf. https://www.ncbi.nlm.nih.gov/books/NBK459183/
- Agana, M., Frueh, J., Kamboj, M., Patel, D. R., & Kanungo, S. (2018). Common metabolic disorder (inborn errors of metabolism) concerns in primary care practice. Annals of translational medicine, 6(24), 469. https://doi.org/10.21037/atm.2018.12.34
- Teixeira, C., Cordeiro, C., Pinto, C., & Diogo, L. (2023). Clinical Presentation of Inherited Metabolic Diseases in Newborns Hospitalised in an Intensive Care Unit. Journal of mother and child, 27(1), 55–63. https://doi.org/10.34763/jmotherandchild.20232701.d-23-00021
- Postępowanie terapeutyczne w hiperamonemii pierwotnej - Standardy Medyczne. (n.d.). Postępowanie Terapeutyczne W Hiperamonemii Pierwotnej - Standardy Medyczne. https://www.standardy.pl/artykuly/id/1205