Wyszukaj w publikacjach
Zespół Nijmegen – konsekwencje immunologiczne i onkologiczne „słowiańskiej mutacji”

Zespół Nijmegen (Nijmegen breakage syndrome, NBS) to rzadkie zaburzenie genetyczne z grupy tzw. niestabilności chromosomowej, dziedziczone w sposób autosomalny recesywny.
Choroba występuje stosunkowo częściej w Europie Środkowo-Wschodniej, w tym w Polsce, z uwagi na efekt założycielski w populacji słowiańskiej. Szacuje się, że 1 na 166 osób w tym regionie jest nosicielami wariantu patogennego.
Podłoże genetyczne mutacji w genie NBN
Zespół Nijmegen spowodowany jest obecnością wariantów patogennych w genie NBN (dawniej NBS1), kodującym białko nibrynę. Nibryna uczestniczy w procesach naprawy DNA, szczególnie w mechanizmach odpowiedzi na podwójne pęknięcia nici DNA. Defekt prowadzi do niestabilności chromosomowej i zwiększonej podatności na uszkodzenia genetyczne indukowane promieniowaniem jonizującym oraz niektórymi cytostatykami.
„Ptasi wygląd” – obraz kliniczny zespołu Nijmegen
Cechy dysmorficzne i rozwój
Większość dzieci rodzi się ze skrajnym małogłowiem. Z czasem obserwuje się charakterystyczny fenotyp, w starszej literaturze porównywany do „ptasiego wyglądu”:
- wydatny nos,
- cofnięty podbródek,
- duże uszy,
- niskie, pochyłe czoło.
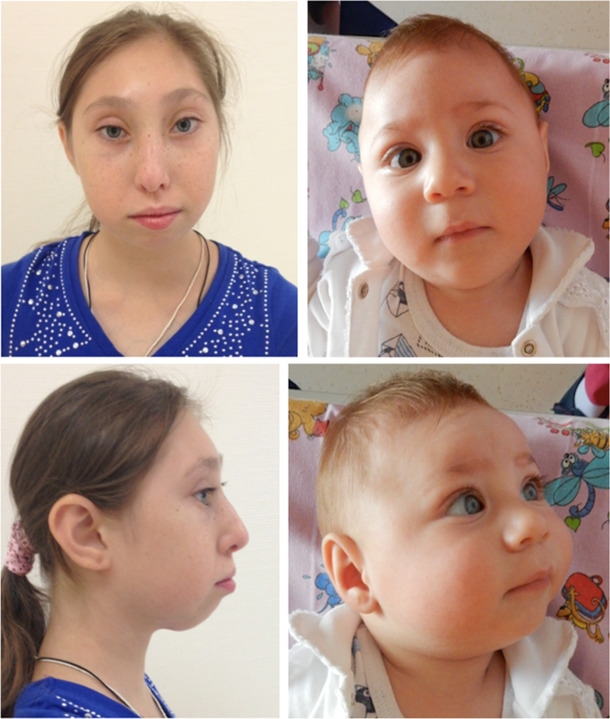
Rozwój intelektualny we wczesnym dzieciństwie mieści się zazwyczaj w granicach normy, jednak z czasem pogarsza się. Umiejętności interpersonalne pacjentów, którzy często są postrzegani przez otoczenie jako pogodni, ale nieco wycofani, pozostają natomiast raczej dobre.
Zaburzenia odporności
Typowy jest niedobór odporności o zmiennym nasileniu. Najczęściej obejmuje deficyt odporności humoralnej (hipogammaglobulinemia, obniżone IgG2, IgA) oraz zwiększoną podatność na infekcje dróg oddechowych i zakażenia układu moczowego. Może przypominać obraz kliniczny złożonego niedoboru odporności (CID).
Należy unikać szczepień szczepionkami żywymi, poza tym realizując kalendarz szczepień. Warto mieć jednak świadomość, że odpowiedź na immunizację może być osłabiona w stosunku do zdrowej populacji.
Nowotwory
Najpoważniejszym powikłaniem jest wysokie ryzyko nowotworów złośliwych, zwłaszcza chłoniaków nieziarniczych (zarówno B-, jak i T-komórkowych). Ryzyko nowotworu sięga nawet 40% w ciągu życia, a pierwsze zachorowania występują często już w wieku dziecięcym. Opisywano także przypadki białaczek, guzów mózgu i innych nowotworów litych.
Ze względu na nadwrażliwość na promieniowanie jonizujące należy jednak – poza bezwzględnymi wskazaniami – unikać w toku diagnostyki wykonywania badań TK i RTG.
Inne objawy
Poza zaburzeniami związanymi z funkcjonowaniem układu odpornościowego, pacjenci z zespołem Nijmegen doświadczają również innych problemów zdrowotnych, które są konsekwencją:
- niskiej masy urodzeniowej,
- hipogonadyzmu i opóźnionego dojrzewania płciowego,
- wad układu kostnego, serca i nerek,
- nadwrażliwości na promieniowanie jonizujące i chemioterapię alkilującą (m.in. cyklofosfamid, ifosfamid, cisplatyna, karboplatyna, melfalan, busulfan, dakarbazyna, temozolomid).
Diagnostyka zespołu Nijmegen
Chociaż charakterystyczne cechy fenotypowe mogą nasuwać silne podejrzenie zespołu Nijmegen, to do postawienia ostatecznego rozpoznania konieczne jest stwierdzenie metodami molekularnymi wariantu patogennego w genie NBN.
Postępowanie i leczenie pacjentów z mutacją w genie NBN
Nie istnieje leczenie przyczynowe zespołu Nijmegen. Terapia jest głównie objawowa i profilaktyczna.
Opieka immunologiczna
- Regularne monitorowanie funkcji odporności.
- Substytucja immunoglobulin u pacjentów z istotnym niedoborem.
- Profilaktyka antybiotykowa przy nawracających infekcjach.
Monitorowanie pod kątem nowotworów
Ze względu na wysokie ryzyko nowotworów konieczna jest czujność onkologiczna: regularne badania obrazowe i laboratoryjne oraz uwzględnianie w diagnostyce różnicowej nowotworów, szczególnie hematologicznych.
Leczenie chłoniaków jest trudne z uwagi na nadwrażliwość na radioterapię i chemioterapię. Standardowe protokoły mogą prowadzić do poważnych powikłań, dlatego leczenie wymaga indywidualizacji. Możliwe jest natomiast zastosowanie megachemioterapii z przeszczepieniem komórek krwiotwórczych, co w przypadku allo-HSCT zapewnia również prawidłową funkcję układu odpornościowego po zakończeniu leczenia onkologicznego.
Opieka wielospecjalistyczna
Zależnie od współistniejących zaburzeń, należy rozważyć również opiekę poradni:
- endokrynologicznej,
- kardiologicznej,
- nefrologicznej,
- rehabilitacyjnej,
- psychologiczno-pedagogicznej.
Długość życia z zespołem Nijmegen
Przebieg choroby jest zróżnicowany. U części pacjentów jakość i długość życia są znacznie ograniczone przez nowotwory lub infekcje o ciężkim przebiegu, inni funkcjonują względnie dobrze w dorosłości. Niestety, mediana przeżycia jest istotnie niższa niż w populacji ogólnej.
Poradnictwo genetyczne dla rodzin pacjentów z mutacjami w NBN
Zespół Nijmegen dziedziczy się w sposób autosomalny recesywny. Oznacza to, że aby doszło do ujawnienia choroby, dziecko musi odziedziczyć dwie nieprawidłowe kopie genu NBN – po jednej od każdego z rodziców. Nosiciele pojedynczej mutacji (heterozygoty) nie wykazują cech zespołu, ale mogą przekazać wadliwy allel potomstwu. Ryzyko urodzenia chorego dziecka wynosi 25% w każdej ciąży w przypadku, gdy oboje rodzice są nosicielami mutacji.
Z uwagi na wysoki odsetek nosicielstwa mutacji c.657_661del5 w populacji środkowoeuropejskiej, w tym w Polsce, poradnictwo genetyczne ma szczególne znaczenie. Rodziny, w których rozpoznano NBS, powinny mieć możliwość skorzystania z konsultacji genetycznej i diagnostyki molekularnej w celu identyfikacji nosicieli mutacji oraz rozważenia badań prenatalnych lub preimplantacyjnych.
Znaczenie dla lekarzy spoza onkologii
Zespół Nijmegen, choć rzadki, powinien być brany pod uwagę w praktyce pediatrycznej. Każde dziecko z mikrocefalią, typowymi cechami dysmorfii i nawracającymi infekcjami wymaga pilnej diagnostyki w kierunku zaburzeń w genie NBN. Świadomość choroby pozwala na szybsze skierowanie do ośrodka specjalistycznego i unikanie potencjalnie niebezpiecznych terapii (np. radioterapii).
Źródła
- Dobrzańska, A., Obrycki, Ł., & Socha, P. (2020). Choroby rzadkie. Standardy medyczne.
- Nijmegen Breakage Syndrome. (2025). Up To Date. uptodate.com/contents/nijmegen-breakage-syndrome [ostatni dostęp: 18.08.2025 r.]
- Varon, R., Demuth, I., & Chrzanowska, K.H. (1999, updated 2023). Nijmegen Breakage Syndrome. In: Adam, M.P., Feldman, J., & Mirzaa, G.M. GeneReviews® [Internet]. Seattle (WA): University of Washington, Seattle; 1993-2025. Available from: https://www.ncbi.nlm.nih.gov/books/NBK1176/ [ostatni dostęp: 18.08.2025 r.]