Wyszukaj w publikacjach
Choroba Perthesa – kiedy podejrzewać martwicę głowy kości udowej u dzieci?
Choroba Perthesa, określana również jako jałowa martwica głowy kości udowej, to schorzenie ortopedyczne typowe dla wieku rozwojowego. Najczęściej występuje u dzieci rasy kaukaskiej w wieku od 3 do 12 lat, ze szczytem zachorowań między 5. a 7. rokiem życia. Zdecydowanie częściej dotyczy chłopców (stosunek 4:1) i zazwyczaj ma charakter jednostronny, choć w 10–24% przypadków obserwuje się obustronne zajęcie stawów biodrowych.
Etiologia choroby Perthesa
Obecnie nie jest znana jednoznaczna przyczyna rozwoju choroby Perthesa. Przyjmuje się, że schorzenie ma podłoże wieloczynnikowe, obejmujące zarówno kwestie genetyczne, jak i środowiskowe.
Wśród potencjalnych mechanizmów sprawczych wymienia się m.in.:
- patologiczny wzrost ciśnienia wewnątrztorebkowego stawu biodrowego,
- zaburzenia w zakresie hormonu wzrostu,
- nieprawidłowości w obrębie płytek wzrostowych,
- anomalie naczyniowe.
Na rozwój choroby mogą również wpływać czynniki środowiskowe, takie jak:
- opóźnione kostnienie nasad kości,
- niska masa urodzeniowa,
- deprywacja psychospołeczna w dzieciństwie,
- palenie tytoniu przez matkę w ciąży,
- otyłość.
Patogeneza choroby Perthesa
Choroba Perthesa charakteryzuje się przede wszystkim zaburzeniem unaczynienia nasady kości udowej, prowadzącym do jałowej martwicy (bez udziału drobnoustrojów). Niedokrwienie skutkuje zapadnięciem się głowy kości udowej, utratą jej kulistości, a w konsekwencji – rozwojem wtórnych zmian zwyrodnieniowych zarówno w obrębie stawu biodrowego, jak i otaczających tkanek.
Proces chorobowy przebiega zazwyczaj w czterech etapach:
- stadium I (martwica) – obumarcie części głowy kości udowej oraz zahamowanie wzrostu nasady;
- stadium II (resorpcja i naprawa) – usuwanie martwej tkanki i procesy regeneracyjne, które mogą prowadzić do deformacji głowy kości;
- stadium III (reosyfikacja) – mineralizacja nowo tworzonej kości oraz ewentualne utrwalenie powstałych deformacji;
- stadium IV (przebudowa i adaptacja) – adaptacja zdeformowanej głowy kości udowej, co często skutkuje jej powiększeniem.
Czas trwania poszczególnych etapów jest zmienny. Szacuje się, że faza martwicy i fragmentacji trwa około 6 miesięcy, etap reosyfikacji od 18 miesięcy do 3 lat, a ostateczna przebudowa może trwać aż do zakończenia dojrzewania kostnego.
Objawy martwicy głowy kości udowej
Najczęstszym powodem zgłoszenia się dziecka do lekarza jest utykanie oraz charakterystyczny chód Trendelenburga. Objawom tym często towarzyszy ból, którego lokalizacja bywa myląca – najczęściej odczuwany jest w okolicy kolana lub uda, a rzadziej bezpośrednio w stawie biodrowym. Ból pojawia się po wysiłku fizycznym i ustępuje w spoczynku, co może przyczyniać się do opóźnienia rozpoznania.
W przebiegu choroby obserwuje się zmniejszoną aktywność ruchową dziecka, które unika chodzenia i coraz częściej utyka. Rodzice często wiążą te objawy z przebytym wcześniej urazem, co dodatkowo może maskować rzeczywistą przyczynę.
W badaniu fizykalnym stwierdza się ból w okolicy pachwiny przy palpacji. Zakres ruchu w stawie kolanowym pozostaje prawidłowy. Typowe są natomiast ograniczenia odwiedzenia oraz rotacji wewnętrznej i zewnętrznej w stawie biodrowym, a także przykurcz zgięciowy.
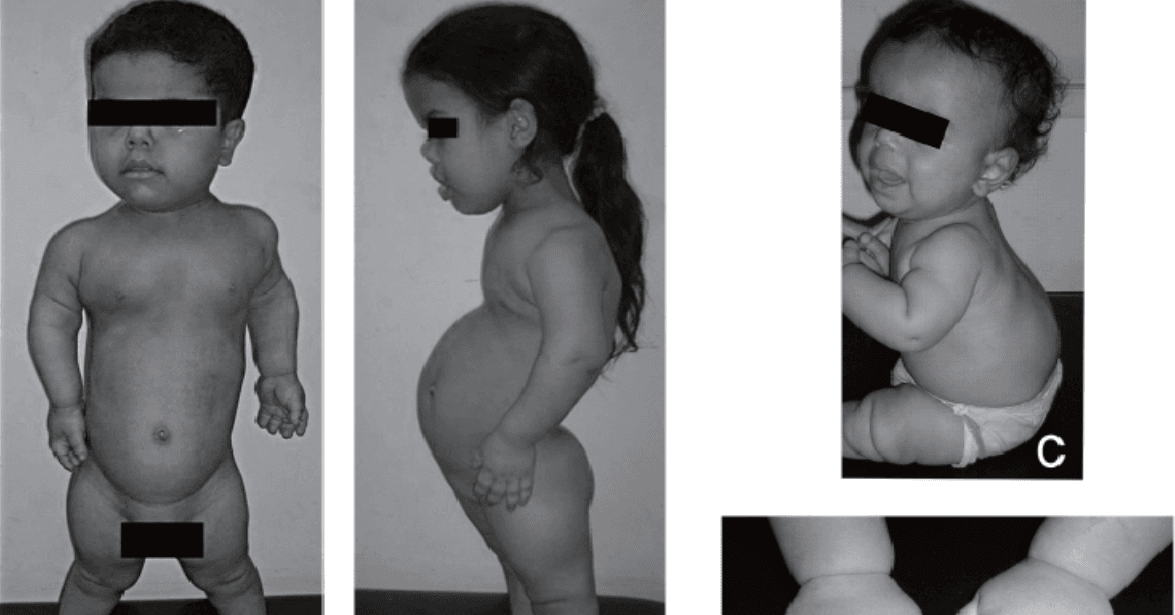
W bardziej zaawansowanych stadiach choroby rozwija się przykurcz przywiedzeniowy, widoczne jest wyszczuplenie uda i pośladka, a także skrócenie kończyny dolnej. Dziecko zwykle cechuje się niskim wzrostem i drobną budową ciała w porównaniu do rówieśników.
Diagnostyka choroby Perthesa
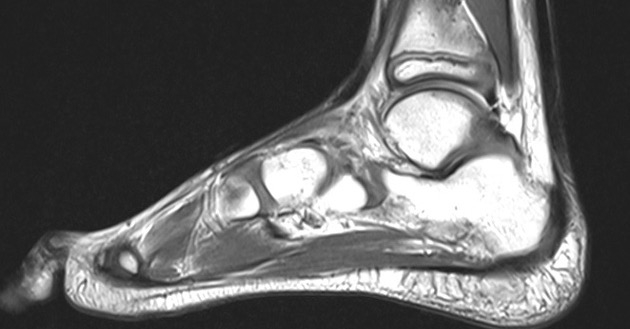
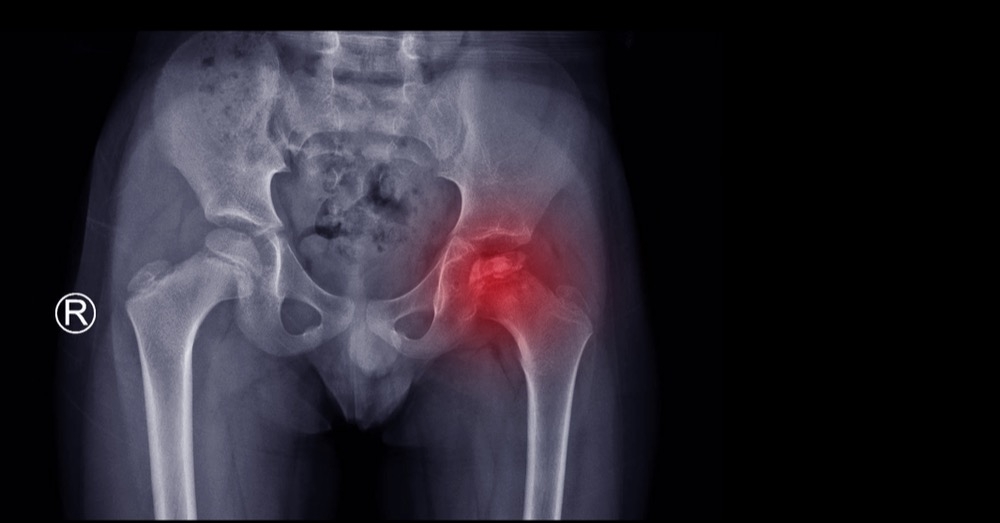
Rozpoznanie choroby Perthesa opiera się przede wszystkim na badaniu rentgenowskim stawu biodrowego wykonywanym w projekcjach przednio-tylnej (A-P) oraz osiowej. Obraz RTG umożliwia ocenę takich zmian jak:
- obniżenie wysokości nasady,
- złamania podchrzęstne,
- fragmentacja tkanki kostnej,
- deformacja głowy kości udowej,
- poszerzenie i skrócenie szyjki kości udowej.
RTG jest także podstawowym narzędziem w ocenie postępów leczenia – zaleca się wykonywanie kontrolnych zdjęć co 4–6 tygodni w fazie rozpoznania oraz co 6 miesięcy w dalszym przebiegu choroby.
W przypadkach wątpliwych lub nietypowych pomocniczo stosuje się inne metody obrazowe, takie jak MRI, TK, USG czy scyntygrafia. W sytuacjach wymagających dokładniejszej oceny struktury stawu, szczególnie przed leczeniem operacyjnym, wykorzystuje się artrografię dynamiczną.
Leczenie jałowej martwicy kości udowej
Leczenie choroby Perthesa ma charakter przyczynowy i koncentruje się na ochronie głowy kości udowej przed deformacją. Kluczowym celem postępowania jest utrzymanie sferycznego kształtu głowy kości udowej oraz zachowanie pełnej ruchomości stawu biodrowego. W realizacji tego celu istotne są:
- rekonstrukcja siły mięśniowej,
- eliminacja czynników ryzyka deformacji,
- oraz – w razie konieczności – leczenie operacyjne.
Wybór metody leczenia zależy od obrazu radiologicznego, wieku szkieletowego oraz stopnia zaawansowania choroby. Leczenie chirurgiczne zazwyczaj nie jest wymagane u pacjentów we wczesnych stadiach, z pełnym i bezbolesnym zakresem ruchu w stawie biodrowym oraz niskim ryzykiem progresji martwicy. Dzieci, u których wiek szkieletowy w momencie rozpoznania wynosi ≤6 lat, zwykle dobrze rokują przy leczeniu zachowawczym.
Leczenie nieoperacyjne
Zalecane głównie w przypadkach o łagodniejszym przebiegu i ograniczonym zakresie martwicy głowy kości udowej. Obejmuje:
- odpoczynek – u pacjentów z bólem lub sztywnością stawu biodrowego zaleca się odpoczynek; w celu łagodzenia objawów można stosować NLPZ;
- hospitalizacja i trakcja – u pacjentów nieodpowiadających na leczenie ambulatoryjne stosuje się obustronną trakcję skórną z postępującym odwiedzeniem, celem odciążenia i unieruchomienia stawu;
- odciążenie kończyny – w codziennym funkcjonowaniu stosuje się kule łokciowe; w okresach zaostrzeń może być konieczne czasowe unikanie obciążania kończyny.
Leczenie operacyjne
Rozważa się u pacjentów w wieku powyżej 6 lat, u których w momencie rozpoznania występuje ponad 50% martwica głowy kości udowej lub gdy leczenie zachowawcze nie przynosi efektu.
Możliwe techniki operacyjne obejmują:
- osteotomię (kości udowej lub miednicy),
- tenotomię przywodzicieli uda – celem poprawy ustawienia głowy kości udowej i warunków biomechanicznych stawu.
Różnicowanie martwicy głowy kości udowej
Rozpoznanie choroby Perthesa, zwłaszcza w jej wczesnym stadium, może nastręczać trudności diagnostycznych ze względu na brak swoistych zmian radiologicznych. W takich przypadkach niezbędne jest uwzględnienie szeregu jednostek chorobowych w diagnostyce różnicowej.
Należy rozważyć:
- przejściowe (jałowe) zapalenie stawu biodrowego,
- młodzieńcze idiopatyczne zapalenie stawów,
- młodzieńcze złuszczenie głowy kości udowej,
- zaburzenia odżywienia nasady bliższego końca kości udowej,
- dysplazje kostno-chrzęstne,
- choroby układowe, w tym hematologiczne, takie jak białaczka czy hemofilia.
Wśród chorób endokrynologicznych mogących dawać podobny obraz kliniczny wymienia się niedoczynność tarczycy. Rzadsze, ale istotne diagnostycznie, są wrodzone wady rozwojowe, takie jak niedorozwój bliższego końca kości udowej, a także zespoły genetyczne – np. zespół Klinefeltera.
Rokowanie w chorobie Perthesa
Najlepsze wyniki leczenia obserwuje się u chłopców oraz u dzieci, które zachorowały przed 8. rokiem życia. Im mniejszy zakres uszkodzenia głowy kości udowej, tym krótszy przebieg choroby i lepsze rokowanie funkcjonalne.
Dane długoterminowe wskazują, że następstwa kliniczne po 40. roku życia są zazwyczaj minimalne, a dobre rokowanie obserwuje się w około 60–80% przypadków. Kluczowym czynnikiem wpływającym na funkcję stawu w dorosłości jest ostateczny kształt i centrowanie głowy kości udowej w panewce. Obecność deformacji głowy kości udowej po zakończeniu procesu chorobowego istotnie zwiększa ryzyko rozwoju wtórnych zmian zwyrodnieniowych. W najbardziej zaawansowanych przypadkach prowadzi to do konieczności całkowitej endoprotezoplastyki stawu biodrowego, co dotyczy około 5% pacjentów.
Źródła
- Kruczyński, J. (2023). Wiktora Degi ortopedia i rehabilitacja (Wyd. 3). Warszawa: PZWL Wydawnictwo Lekarskie. ISBN 978-83-01-23058-6.
- Rodríguez-Olivas, A. O., Hernández-Zamora, E., & Reyes-Maldonado, E. (2022). Legg-Calvé-Perthes disease overview. Orphanet journal of rare diseases, 17(1), 125. https://doi.org/10.1186/s13023-022-02275-z
- Pavone, V., Chisari, E., Vescio, A., Lizzio, C., Sessa, G., & Testa, G. (2019). Aetiology of Legg-Calvé-Perthes disease: A systematic review. World journal of orthopedics, 10(3), 145–165. https://doi.org/10.5312/wjo.v10.i3.145